Perubahan kimia atau yang disebut reaksi kimia biasanya ditulis dalam bentuk persamaan reaksi. Dalam persamaan reaksi selalu diberi koefisien yang sesuai untuk memenuhi hukum kekekan massa dan teori atom Dalton. Salah satu postulat atom Dalton menyatakan jenis dan jumlah atom yang terlibat dalam reaksi kimia biasa (tidak melibatkan reaksi fisi dan fusi) tidak berubah tetapi hanya mengalami penataan ulang. Sebenarnya hal postulat atom Dalton ini hanya menjelaskan hukum kekekalan massa.
Contoh 1
Logam aluminium bereaksi dengan gas O2 membentuk aluminium oksida. Tulislah persamaan reaksi dan penyetaraannya?
1) Menulis rumus kimia atau lambang unsur dari reaktan dan produk dengan wujud masing-masing spesies.
Al(s) + O2(g)→Al2O3(s)
2) Tetapkan koefisien salah satu spesi sama dengan 1 (biasanya spesi yang rumus kimianya lebih kompleks).
Pada reaksi di atas spesi yang lebih kompleks adalah Al2O3 = 1
3) Setarakan unsur yang terkait langsung dengan zat yang telah diberi koefisien 1.
Koefisien Al2O3 = 1
Maka Al diruas kanan = 2
Al diruas kiri = 1
Agar jumlah atom Al pada kedua ruas sama maka Al pada ruas kiri diberi kofisien 2. Persamaan reaksinya menjadi:
2Al(s) + O2(g) → Al2O3(s)
Atom O
Koefisien Al2O3 = 1
atom O diruas kanan = 3
Jumlah atom O diruas kiri = 2
Agar jumlah atom O pada kedua ruas sama maka atom O pada ruas kiri diberi koefisien 3/2. Persamaan reaksinya menjadi:
2Al(s) + 3/2O2(g) → Al2O3(s)
Agar koefisien tidak dalam bentuk pecahan koefisien pada kedua ruas dikalikan dengan satu bilangan agar diperoleh suatu bilangan bulat. Untuk memperoleh bilangan bulat maka kedua ruas dikali 2, sehingga diperoleh persamaan reaksi yang setara dengan koefisien dalam bentuk bilangan bulat:
4Al(s) + 3O2(g) → 2Al2O3(s)
4) Biasanya oksigen disetarakan paling terakhir jika masih terdapat unsur-unsur lain.
Contoh 2
Reaksi besi(III) oksida dengan larutan asam sulfat membentuk besi(III) sulfat dan air. Tulislah persamaan reaksi dan setarakan persamaan reaksi tersebut?
Jawab
1. Menulis rumus kimia atau lambang unsur dari reaktan dan produk dengan wujud masing-masing spesies.
FeO3(s) + H2SO4 → Fe(SO4)3(aq) + H2O(l)
2. Tetapkan koefisien salah satu spesi sama dengan 1 (biasanya spesi yang rumus kimianya lebih kompleks). Sedangkan koefisien yang lainnya disetarakan huruf sebagai kofisien sementara.
Koefisien Fe2(SO4)3 = 1 dan koefisien yang lain menggunakan huruf. Persamaan reaksi menjadi:
aFeO3(s) + bH2SO4 → 1Fe(SO4)3(aq) + cH2O(l)
3. Setarakan unsur yang terkait langsung dengan zat yang telah diberi koefisien 1.
Dari reaksi tersebut unsur yang berikAtan langsung dengan zat telah diberi koefisien 1 adalah Fe, S dan O. Namun O disetarakan terakhir karena unsur O terdapat di lebih dari dua zat.
Penyetaraan atom Fe
Jumlah atom Fe di ruas kiri = 2a
Jumlah atom Fe di ruas kanan = 2
Maka jumlah atom Fe diruas kiri atau harga koefisien a = 2a = 2, a = 1
Penyetaraan atom S
Jumlah atom S di ruas kiri = b
Jumlah atom S di ruas kanan = 3
Maka jumlah atom S di ruas kiri atau harga koefisien b = 3
Persamaan reaksinya menjadi:
1FeO3(s) + 3H2SO4 → 1Fe(SO4)3(aq) + cH2O(l)
4. Setarakan atom lainnya. Atom O disetarakan setelah semua atom setara.
Penyetaraan atom H
Jumlah atom H di ruas kiri = 6
Jumlah atom H di ruas kanan = 2c
Maka jumlah atom H di ruas kanan atau harga koefisien b = 2c = 6, c = 3
Persamaan reaksinya menjadi:
1FeO3(s) + 3H2SO4 → 1Fe(SO4)3(aq) + 3H2O(l)
5. Setarakan atom O. Karena semua atom telah setara, maka oksigen seharusnya telah setara juga. Untuk meyakinkan jumlah atom O pada kedua ruas telah setara, maka dilakukan penjumlahan atom O pada kedua ruas.
Jumlah atom O di ruas kiri = 3 + 12 = 15
Jumlah atom O di ruas kanan = 12 + 3 = 15.
Dari penjumlahan ini, terbukti jumlah atom O pada ruas kiri dan ruas kanan telah setara. Jadi persamaan reaksi setaranya adalah sebagai beriktu:
FeO3(s) + 3H2SO4 → Fe(SO4)3(aq) + 3H2O(l)
Contoh 3
Reaksi antara tembaga dengan larutan asam nitrat encer menghasilkan tembaga(II) nitrat, gas nitrogen monoooksida dan air. Tulislah persamaan reaksi dan setarakan persamaan reaksi tersebut?
Jawab
1. Menulis rumus kimia atau lambang unsur dari reaktan dan produk dengan wujud masing-masing spesies.
Cu(s) + HNO3(aq) → Cu(NO3)2(aq) + NO(g) + H2O(l)
2. Tetapkan koefisien salah satu spesi sama dengan 1 (biasanya spesi yang rumus kimianya lebih kompleks). Sedangkan koefisien yang lainnya disetarakan huruf sebagai kofisien sementara.
Koefisien Cu(NO3)2 = 1, dan koefisien yang lain menggunakan huruf. Persamaan reaksi menjadi:
aCu(s) + bHNO3(aq) → 1Cu(NO3)2(aq) + cNO(g) + dH2O(l)
3. Setarakan unsur yang terkait langsung dengan zat yang telah diberi koefisien 1.
Pada reaksi di atas, hanya Cu yang dapat langsung disetarakan yaitu a = 1. Untuk unsur yang lainnya walaupun terkait langsung dengan Cu(NO3)2 tetapi tidak dapat langsung disetarakan karena terdapat di lebih dari dua zat yang belum mempunyai harga korfisien. Maka untuk menyetarakannya ikuti persamaan-persamaan berikut:
· Menyetarakan atom N → b = 2 + c ……………………… (1)
· Menyetarakan atom H → b = 2d …………………………. (2)
· Menyetarakan atom O → 3b = 6 + c + d ……………… (3)
Dari persamaan-persamaan di atas nyatakan nilai c dan d dalam b, sebagai berikut:
· Dari persamaan (1), b = 2 + c → c = b – 2
· Dari persamaan (2), b = 2d → d = 0,5 b
Substitusikan nilai c dan d ke dalam persamaan (3)
3b = 6 + c + d
3b = 6 + (b – 2) + (0,5 b)
1,5b = 4
b = 
nilai b yang telah diperoleh di substitusikan ke persamaan (1) dan (2) untuk memperoleh nilai c dan d. Maka nilai c dan d berturut-turut adalah
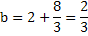
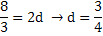
persamaan reaksinya menjadi:
1Cu(s) + 8/3HNO3(aq) → 1Cu(NO3)2(aq) + 2/3NO(g) + 4/3H2O(l)
karena masih dalam bentuk pecahan maka dikalikan 3 agar diperoleh koefisien dalam bentuk bilangan bulat.
3Cu(s) + 8HNO3(aq) → 3Cu(NO3)2(aq) + 2NO(g) + 4H2O(l)
Jumlah atom di produk dan reaktan
|
Atom
|
Reaktan
|
Produk
|
|
Cu
|
3
|
3
|
|
H
|
8
|
8
|
|
N
|
8
|
8
|
|
O
|
24
|
24
|





