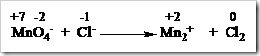
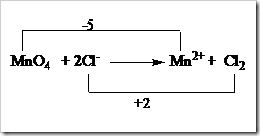
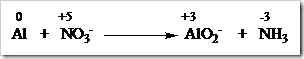
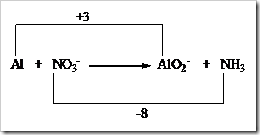
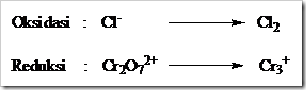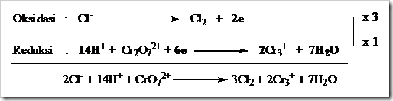Dalam laboratorium terdapat beberapa zat yang dapat digunakan sebagai oksidator. Oksidator yaitu zat yang dapat menyebabkan zat lain mengalami oksidasi sehingga dirinya sendiri akan mengalami reduksi. Umumnya unsur-unsur nonlogam merupakan oksidator yang baik karena memiliki keelektronegatifan tinggi sehingga mudah menangkap atau menarik elektron kearah dirinya. Walaupun demikian tidak selalu digunakan unsur dalam semua reaksi kimia.
Dalam laboratorium terutama reaksi redoks yang dilangsungkan dalam bentuk larutan yang biasa digunakan sebagai oksidator adalah ion permangananat (MnO4–), ion kromat (CrO42-), ion kromat (Cr2O72-). Ketiga zat tersebut merupakan oksidator yang kuat dan mudah melepas oksigen sehingga penanganannya perlu berhati-hati. Zat-zat ini harus disimpan ditempat tersendiri dan tidak boleh berada di dekat zat-zat organik karena dapat menyebabkan kebakaran.
Bila mengenai anggota segera bilas dengan air yang mengalir. Bila mengenai mata segera rendam mata dalam air, hal ini dapat dilakukan dengan cara membuka mata dalam aquades yang disimpan dalam baskom atau ember besar. Setelah itu segera di bawa ke dokter atau memberi obat tetes mata. Bila sampai tertelan segera minum air sebanyak-banyaknya untuk mengencerkan zat kimia yang tertelan lalu segera di bawa ke dokter. Oleh sebab itu, dalam melakukan praktikum jangan pernah mengambil semua larutan dengan cara menyedot.
ION PERMANGANANAT (MnO4–)
Ion permanganat berwarna ungu demikian pula larutan yang mengandung ion permanganat. Warna tersebut merupakan ciri khas dari ion permanganat. Biasanya dalam laboratorium ion permanganat diperoleh dari garam kalium permanganat (KMnO4). KMnO4 merupakan suatu kristal berwarna hitam keunguan.



Gambar Kristal kalium permanganat dan larutan kalium permanganat
Bila terkena cahaya atau dipanaskan pada suhu 230°C, kalium permanganat akan terurai sesuai reaksi berikut.
2 KMnO4 → K2MnO4 + MnO2 + O2
Bilangan oksidasi mangan dalam KMnO4 adalah +7. Ketika terjadi reaksi kimia bilangan oksidasi mangan turun atau mengalami reduksi. Reaksi reduksi mangan dalam KMnO4 bergantung pada keasaman larutan. Dalam suasana larutan asam kuat mangan direduksi menjadi Mn2+ dan warna larutan memudar (hampir tidak berwarna). Setengah reaksi reduksi ion permanganat dalam suasana asam.
8H+ + MnO4– + 5e → Mn2+ + 4H2O
Dalam suasana netral atau sedikit basa ion MnO4– direduksi menjadi MnO2 yang tidak larut dalam larutan atau membentuk endapan. Oleh sebab itu dalam melakukan titrasi pada suasana basa atau suasana alkalis, larutan yang mengandung ion MnO4– tidak disarankan karena endapan MnO2 yang terbentuk dapat mengaburkan titik akhir titrasi. Setengah reaksi reduksi ion permanganat dalam suasana netral atau alkalis.
2H2O + MnO4– + 3e → MnO2 + 4OH–
Untuk membuat suasana asamsebaiknya dipakai asam sulfat, karena asam ini tidak menghasilkan reaksi samping. Sebaliknya jika dipakai asam klorida dapat terjadi kemungkinan teroksidasinya ion klorida menjadi gas klor dan reaksi ini mengakibatkan dipakainya larutan permanganat dalam jumlah berlebih. Meskipun untuk beberapa reaksi dengan arsen(III) oksida, antimon(II) dan hidrogen peroksida, karena pemakaian asam sulfat justru akan menghasilkan beberapa tambahan kesulitan.
Kalium pemanganat adalah oksidator kuat, oleh karena itu jika berada dalam HCl akan mengoksidasi ion Cl– yang menyebabkan terbentuknya gas klor dan kestabilan ion ini juga terbatas. Biasanya digunakan pada medium asam 0,1 N. Namun, beberapa zat memerlukan pemanasan atau katalis untuk mempercepat reaksi. Seandainya banyak reaksi itu tidak lambat, akan dijumpai lebih banyak kesulitan dalam menggunakan reagen ini.
Reaksi reduksi ion permanganat juga dapat berlangsung dalam suasana netral dan basa kuat, Perekasi kalium permanganat tidak merupakan pereaksi baku primer. Sangat sukar untuk mendapatkan pereaksi dalam keadaan murni, bebas dari mangan(IV) oksida (mangan dioksida). Lagi pula air dipakai sebagai pelarut sangat mungkin masih mengandung zat pengotor lain yang dapat mereduksi permanganat menjadi mangan dioksida.
Timbulnya mangan dioksida justru akan mempercepat reaksi reduksi permanganat. Demikian juga adanya ion mangan(II) dalam larutan akan mempercepat reduksi permanganat menjadi mangan dioksida, reaksi tersebut berlangsung sangat cepat dalam suasana netral. Dengan adanya alasan-alasan tersebut maka pembuatan larutan baku permanganat dilakukan sebagai berikut. Larutkan sejumlah(gram) pereaksi dalam air kemudian didihkan selama satu jam diatas penangas air. Selanjutnya disaring lewat penyaring yang bebas dari zat pereduksi.
Wadah bertutupkan sumbat kaca yang dipakai untuk menyimpan larutan, harus benar-benar bebas dari zat pengotor seperti lemak atau zat pengotor lain. Untuk keperluan ini biasanya wadah tersebut dicuci bersih memakai campuran larutan kalium dikromat dan asam sulfat pekat, diikuti pembilasan dengan aquades. Larutan ini sebaiknya disimpan ditempat gelap, terhindar dari cahaya, karena itu sebaiknya dipakai botol berdinding gelap.
Reaksi asam sulfat pekat dengan KMnO3 membentuk Mn2O7. Reaksi ini berlangsung sangat eksotermsis dan dapat meledak. Demikian juga dengan asam klorida membentuk gas glor yang sangat beracun. Reaksi antara asam nitrat dengan alkena akan memutuskan ikatan rangkap dua dan diperoleh suatu asam karboksilat.
CH3(CH2)17CH=CH2 + 2KMnO4 + 3H2SO4 → CH3(CH2)17COOH + CO2 + 4H2O + K2SO4 + 2MnSO4
KMnO4 juga dapat mengoksidasi aldehida menjadi asam karboksilat. Misalnya mengoksidasi n-heptanal menjadi asam heptanoat.
5C6H13CHO + 2KMnO4 + 3 H2SO4 → 5C6H13COOH + 3H2O + K2SO4 + 2MnSO4
Selain itu KMnO4 juga dapat mengoksidasi gugus metil yang terikat pada cincin benzena. Misalnya mengoksidasi toluena menjadi asam benzoat.
5C6H5CH3 + 6KMnO4 + 9H2SO4 → 5C6H5COOH + 14H2O + 2K2SO4 + 6MnSO4
ION KROMAT (CrO42-) DAN DIKROMAT (Cr2O42-)
Dalam laboratorium pasti dijumpai garam yang mengandung ion kromat dan dikromat. Garam yang sering dijumpai yaitu kaliium dan natrium kromat atau dikromat dengan rumus kimia Na2CrO7 (natrium kromat), K2CrO7 (kalium kromat) dan Na2Cr2O7 (natrium dikromat), K2Cr2O7 (kalium dikromat).

Gambar Empat larutan kromium. Dari kiri: larutan yang berwarna kuning adalah kalium dikromat (K2Cr2O7, orange) dan natrium kromat (Na2CrO4), hijau adalah kromium(III) klorida (CrCl3), ungu adalah kromium(III) nitrat (Cr(NO3)3).





Gambar Kristal beberapa senyawa kromium. Dari kiri ke kanan : Natrium kromat tetrahidrat (Na2CrO4·4H2O), kalium dikromat (K2Cr2O7), amonium dikromat ((NH4)2Cr2O3), kromium trioksida (CrO3), kromium oksida (Cr2O3)
(sumber gambar : http://en.tjfuqiang.com/)
Baik ion kromat maupun dikromat mengandung kromium dengan bilangan oksidasi +6 yang merupakaan keadaan oksidasi tertinggi dari krom dalam senyawaaannya. oleh sebab itu dalam reaksi kimia ion kromat dan dikromat akan mengalami reaksi reduksi. Reaksi reduksi ion kromat dan dikromat bergantung pada keasaman larutan.
Warna kuning merupakan ciri khas adanya ion kromat dalam larutan sedangkan warna merah merupakan ciri khas adanya ion dikromat. Larutan yang mengandung ion kromat yang berwarna kuning bila diasamakan, akan diperoleh larutan yang berwarna merah jingga karena ion CrO42- berubah menjadi Cr2O72-.
2CrO42- + 2H+ → Cr2O72- + H2O
Sebaliknya jika larutan yang mengandung ion dikromat dibasakan maka ion Cr2O72- berubah menjadi ion CrO42-.
Cr2O72- + 2OH– → 2CrO42- + H2O
Oleh sebab itu, jika reaksi berlangsung dalam suasana asam yang bertindak sebagai oksidator adalah Cr2O72- dan sebaliknya bila reaksi dilangsungkan dalam suasana basa yang bertindak sebagai oksidator adalah CrO42-.
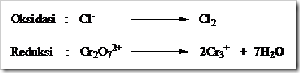
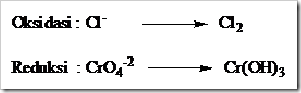
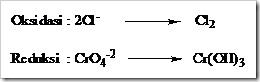
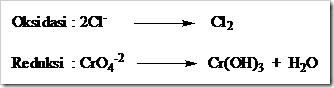
Dalam reaksi kimia bila ion kromat dan dikromat bertindak sebagai oksidator (ketika direaksikan dengan suatu reduktor) bilangan oksidasi kromium turun menjadi +3 dan produk yang diperoleh bergantung pada keadaan keasaman larutan.
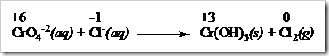
Dalam larutan asam ion kromium direduksi menjadi ion Cr3+, dalam larutan sedikit basa produk reduksinya adalah Cr(OH)3 yang tidak larut dan dalam larutan sangat basa ion kromat direduksi menjadi ion kromit (CrO2–). Persamaan reaksi yang terjadi sebagai berikut.
Larutan asam
6e + 14H+ + Cr2O7 → 2Cr3+ + 7H2O
Larutan sedikit basa
3e + 4H2O + CrO42- → Cr(OH)3 + 5OH–
Larutan sangat basa
3e + 2H2O + CrO42- → CrO2– + 4OH–
Baik Na2CrO7 (natrium kromat), K2CrO7 (kalium kromat), Na2Cr2O7 (natrium dikromat) mapun K2CrO7 (kalium dikromat) bersifat higoskopis sehingga dapat membentuk tetra-, heksa-, dan dekahidrat.
Natrium kromat (Na2CrO4) digunakan sebagai inhibitor korosi dalam industri minyak bumi, sebagai reagen pencelupan dalam industri tekstil, sebagai pengawet kayu. Dengan memanfaatkan isotop Cr-51 dengan waktu paruh 27,8 hari, larutan natrium kromat (VI) digunakan dalam obat-obatan untuk penentuan volume sirkulasi sel darah merah, waktu kelangsungan hidup sel dan evaluasi kehilangan darah.
Campuran kalium dikromat dengan asam nitrat 35% diperoleh suatu larutan yang disebut larutan Schwerter’s yang digunakan untuk menguji keberadaan berbagai logam terutama perak. Perak murni mengubah larutan menjadi merah terang, perak sterling (paduan 92,5% perak dengan logam lain biasanya tembaga atau emas) mengubah larutan menjadi merah gelap, larutan menjadi berwarna coklat bila kandungan tembaga tinggi bahkan menjadi hijau.
SUMBER
James E. Brady. Kimia universitas asas dan struktur edisi keliama jilid 1.
Vogel Analisis Anorganik Kualitatif Makro Dan Semimikro (terjemahan Setiono & Pudjaatmaka) Edisi kelima.
Underwood, A. L & R. A Day, Jr. 1999. Analisis Kimia Kuantitatif (terjemahan A. Hadyana Pudjaatmaka) Edisi kelima. Jakarta: Penerbit Erlangga.
Devy Agustyaningsih. 2010. Penetapan Kadar Kalium Permanganat Menggunakan Fotometer Sederhana Berbasis LED dan CdS Fotosel Detektor. Skripsi Universitas Negeri Malang Fakultas Matematika dan Ilmu Pengetahuan Alam Program Studi Kimia.
Sumber internet
Wikipedia.org
uncp.edu/home/mcclurem/ptable/chromium/cr.htm