Istilah molekul hanya ditujukan pada atom-atom yang berikatan secara kovalen. Ikatan kovalen disebut gaya intramolekul (intramoleculer force) yang mengikat atom-atom menjadi satu kesatuan.
Gaya intramolekul menstabilkan molekul secara individual. Satu molekul dengan molekul lain yang sejenis atau berbeda dapat mengadakan interaksi atau tarik menarik. Gaya tarik menarik antarmolekul-molekul ini disebut gaya antarmolekul atau gaya intermolekul (intermoleculer force).
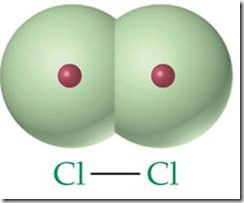
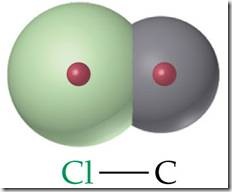
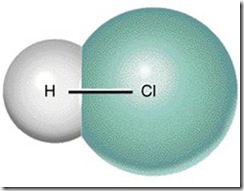
Gaya antar molekul pada umumnya lebih lemah dibandingkan dengan ikatan kovalen. Misalnya untuk memutuskan gaya tarik antara molekul HCl dengan molekul HCl lain, hanya diperlukan energi sebesar 16 kJ/mol, sedangkan untuk memutuskan ikatan kovalen antara atom H dan Cl pada molekul HCl dibutuhkan energi sebesar 431 kJ/mol. Ikatan kovalen dan gaya antarmolekul pada molekul HCl seperti tertera pada Gambar.

Gambar ikatan kovalen (gaya intramolekul) dan gaya antarmolekul dalam molekul-molekul HCl
Secara garis besar terdapat tiga jenis gaya tarik antarmolekul, yaitu
1. Gaya antar molekul nonpolar yaitu gaya dipol sesaat dengan dipol terimbas
2. Gaya antamolekul polar yaitu gaya dipol-dipol
3. Ikatan hidrogen disebut juga gaya dipol-dipol karena molekul yang memiliki ikatan hidrogen selalu berupa molekul polar.
Semua gaya antarmolekul disebut gaya Van Der Waals. Namun terkadang ikatan hidrogen tidak disebut sebagai gaya Van der Waals, walaupun molekul yang memiliki ikatan hidrogen selalu bersifat polar.
Hal ini disebabkan molekul-molekul yang memiliki hidrogen menunjukan sifat yang berbeda dengan molekul lain yang memiliki gaya antarmolekul lain yang massa molekul relatifnya (Mr) sama atau hampir sama.
Gaya Antar Molekul Nonpolar
Gaya tarik antarmolekul nonpolar pertama kali diuraikan oleh ilmuwan fisika, berasal dari Jerman, Fritz London, pada tahun 1930-an sehingga sering disebut gaya London, dan sering pula disebut gaya dispersi.
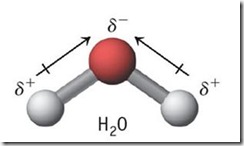
Molekul nonpolar penyebaran elektron dapat dianggap merata, sehingga molekul nonpolar digambarkan berbentuk bola dengan muatan positif dan negatif berimpit pada pusat bola seperti yang ditunjukan pada Gambar.

Seperti yang diketahui elektron dalam molekul selalu dalam keadaan bergerak dan posisinya tidak dapat ditentukan secara pasti akibat berlakunya azas ketidakpastian heisenberg.
Gerakan elektron menyebabkan pada saat-saat tertentu dalam waktu yang sangat singkat penyebaran elektron yang awalnya merata menjadi tidak merata sehingga molekul yang awalnya tidak memiliki dipol menjadi menjadi memiliki dipol atau menyebabkan muatan positif dan negatif yang awalnya berimpit dipusat bola menjadi memisah. Dipol yang timbul dalam waktu yang sangat singkat kemudian kembali lagi ke keadaan awal atau hilang. Karena hal inilah dipol yang timbul disebut dipol sesaat.
Dipol sesaat yang timbul pada satu molekul, tentu saja akan mempengaruhi molekul tetangganya. Oleh sebab itu jika satu molekul mengalami dipol sesaat, maka akan mempengaruhi molekul yang paling dekat dengan dirinya sehingga timbul dipol juga atau muatan positif dan negatif yang awalnya berimpit menjadi memisah juga.
Atau dapat dikatakan molekul yang mengalami dipol sesaat akan mengimbas atau menginduksi molekul-molekul yang berada di dekatnya. Karena hal inilah maka gaya antar molekul nonpolar disebut sebagai gaya dipol sesaat-gaya dipol terimbas atau terinduksi.
Proses pembentukan dipol sesaat dan dipol induksian pada atom Ne yang memiliki dua elektron ditunjukan pada Gambar.

Keterangan angka-angka pada molekul
-
Nomor 1 molekul dengan dua elektron yang selalu dalam keadaan bergerak
-
Nomor 2 molekul yang telah mengalami dipol sesaat
-
Nomor 3 molekul yang telah mengalami dipl sesaat karena diimbas diinduksi oleh molekul nomor 2.
Gaya tarik antara molekul yang memiliki dipol sesaat dengan molekul yang memiliki dipol imbasan inilah yang disebut gaya London.
Kemudahan suatu molekul untuk membentuk dipol sesaat ditunjukan dengan kebolehpolarran. Makin banyak elektron molekul memiliki kebolehpolaran yang besar atau makin mudah mengalami dipol sesaat. Jumlah elektron berbanding lurus dengan massa atom dan massa molekul relatif.
Oleh sebab itu dapat dapat disimpulkan bahwa makin tinggi massa molekul relatif atau massa atom relatif suatu molekul maka makin mudah mengalami dipol sesaat atau gaya london yang terjadi makin kuat.
Adanya gaya London antara molekul-molekul nonpolar menyebabkan pada waktu peleburan dan pendidihan diperlukan sejumlah energi untuk memperbesar jarak antara molekul-molekul nonpolar. semakin kuat gaya London antara molekul-molekul semakin besar pula energi yang diperlukan untuk terjadinya peleburan dan pendidihan.
Gaya Antarmolekul Polar
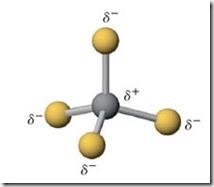
Gaya tarik antar molekul polar disebut gaya tarik dipol-dipol. Hal ini disebabkan molekul polar memiliki penyebabran elektron yang tidak merata sehingga memiliki dipol yang tetap, tidak seperti pada molekul nonpolar yang dipolnya muncul pada saat-saat tertentu saja.
Molekul-molekul polar yang memiliki fasa cair jika berada pada satu tempat, maka molekul-molekul yang ada akan menyusun diri sehingga dipol positif (muatan positif) dekat dengan dipol negatif, begitupun sebaliknya dipol negatif akan menyusun diri agar lebih dekat dengan dipol positif dari molekul tetangganya, seperti yang ditunjukan pada Gambar.

Gambar Gaya tarik dan gaya tolak antara molekul-molekul polar
Dengan posisi seperti ini gayaa tarik yang terjadi lebih kuat dibanding tolaknya. Karena dalam fasa cair molekul–molekul selalu bergerak dan bertumbukan satu dengan yang lain, maka posisi molekul-molekul selalu berubah namun pusat muatan positif dari satu molekul selalu berdekatan dengan pusat muatan negatif molekul-molekul yang lain, begitupun sebaliknya.
Kenaikan energi termal (kenaikan suhu) menyebabkan tumbukan antarmolekul sering terjadidan susunan molekul-molekul menjadi semakin acak (random). Kekuatan gaya tarik antara molekul-molekul semakin berkurang sedangkan kekuatan gaya tolaknya bertambah, akan tetapi kekuatan gaya tarik masih lebih dominan daripada gaya tolak.
Pada waktu temperatur mencapai titik didih cairan maka kekuatan antara gaya tarik dan gaya tolak adalah seimbang, cairan mulai mendidih. Titik didih berkaitan dengan energi yang diperlukan untuk memutuskan gaya antarmolekul bukan memutuskan ikatan antaratom. Semakin kuat gaya antarmolekul, semakin besar energi yang diperlukan untuk memutuskannya.
Dalam fasa padat susunan molekul-molekul polar lebih teratur dibanding dalam fasa cair seperti yang ditunjukan pada Gambar berikut.

Gambar Susunan molekul polar dalam fasa padat
Ikatan Hidrogen
Ikatan hidrogen merupakan gaya antar molekul polar yang paling kuat dibanding dua gaya lainnya. Ikatan hidrogen hanya terbentuk jika hidrogen di ikat oleh dua atom (selama ini hanya dua) yang berkeelektronegatifan tinggi, seperti yang ditunjukan pada gambar.

Atom-atom yang berkeelektronegatifan tinggi tersebut yaitu N, O dan F. Jadi dapat disimpulkan bahwa ikatan hidrogen hanya terbentuk bila molekul tersebut memiliki ikatan
N–H, O–H dan O–F.
Pada gambar di atas jika A adalah N maka B dapat berupa N, O atau F selain ketiga atom tersebut maka ikatan yang terbentuk bukan merupakan ikatan hidrogen. Dilihat dari panjang ikatan, ikatan hidrogen selalu lebih panjang daripada ikatan kovalen.
Contoh senyawa yang memiliki ikatan hidrogen yaitu molekul H2O, HF dan NH3. Dalam fasa cair H2O dengan dua atom hidrogen dan 2 PEB mampu membentuk 4 atom hidrogen antarmolekul dengan 4 molekul H2O lain yang ada di dekatnya seperti yang ditunjukan pada Gambar.

Gambar ikatan hidrogen antar molekul H2O
Pada molekul HF dengan satu atom hidrogen dan 3 PEB (pasangan elektron bebas) dan NH3 dengan 3 atom hidrogen dan 1 PEB hanya mampu membentuk 2 ikatan hidrogen dengan 2 molekul sejenis yang ada di dekatnya.

Gambar Ikatan hidrogen molekul HF yang berbentuk zig-zag
Berdasarkan perbedaan keelktronegatifan atom N, O dan F diketahui bahwa kelektronegatifan F > O > N maka ikatan hidrogen yang dibentuk
H- – F > O- -H > N – – H (keterangan : – – = ikatan hidrogen)
Walaupun demikian diperoleh bahwa titik didih H2O > HF > NH3. Hal ini disebabkan oleh banyaknya ikatan hidrogen yang terbentuk. Ikatan hidrogen molekul air lebih banyak dibanding ikatan hidrogen HF dan NH3. Sedangkan titik didih HF > NH3 karena F lebih elektronegatif dibanding N sehingga ikatan hidrogennya antar molekul lebih kuat.
Dalam fasa padat H2O tetap membentuk 4 ikatan hidrogen, demikian juga untuk HF dan NH3 tetap membentuk 2 ikatan hidrogen dengan dua molekul lain yang ada di dekatnya. Walaupun demikian pada keadaan padat titik lebur H2O > NH3 > HF. Hal ini terjadi dimungkinkan karena kemasan molekul-molekul tersebut dalam kristalnya.
Ikatan hidrogen pada air cair inilah yang menyebabkan air mendidih pada suhu 100°C walaupun massa molekul relatif air hanya 18. Sebagai perbandingan perhatikan titik didih beberapa senyawa berikut.
|
Senyawa
|
Massa molekul relatif (Mr)
|
Titik didih (°C)
|
|
H2O
H2S
H2Se
H2Te
|
18
34
81
130
|
100
-65
-45
-15
|
Ikatan hidrogen digolongkan menjadi dua jenis yaitu
1. Ikatan hidrogen intermolecule atau antarmolekul. Ikatan hidrogen yang terbentuk dari satu molekul dengan molekul tetangganya. Contohnya ikatan hidrpgen pada molekul H2O, HF dan NH3 yang telah dijelaskan di atas.
2. Ikatan hidrogen intramolekul atau ikatan hidrogen dalam satu molekul. Contoh ikatan hidrogen pada molekul asam benzoat seperti yang ditunjukan pada gambar berikut.

Ikatan hidrogen antarmolekul dalam fasa cair dipengaruhi oleh konsentrasi artinya semakin besar konsentrasi semakin semakin kuat ikatan hidrogen yang terbentuk, sedangkan ikatan hidrogen intramolekul tidak dipengaruhi oleh jonsentrasi zat.
Gaya Antar Molekul Polar atau Molekul Nonpolar dengan Ion
Bila suatu ion dilarutkan dalam suatu pelarut polar, maka ion positif (kation) akan didekati oleh dipol negatif dari molekul polar, begitupun sebaliknya ion negatif (anion) akan didekati oleh dipol positif dari molekul polar, seperti yang ditunjukan pada Gambar.

Gambar Gaya tarik antara molekul polar dengan kation dan anion
Jika ion dimasukan ke dalam suatu molekul nonpolar, maka pembentukan dipol sesaat dan dipol induksian dapat terjadi dengan karena:
1. gerakan elektron dalam molekul itu sendiri
2. diinduksi oleh molekul yang telah mengalami dipol sesaat atau disebabkan oleh dipol sesaat dari molekul pada nomor 1.
3. Karena diinduksi oleh ion baik anion maupun kation
4. Molekul nomor 3 dapat menginduksi molekul lain yang ada di dekatnya sehingga mengalami dipol induksian, demikian seterusnya.
Susunan molekul yang mengalmi dipol sesaat dan dipol terimbas sama seperti pada molekul polar yaitu dipol sesaat atau dipol induksi yang bermuatan positif (ujung positif) lebih mengarah ke anion dan begitupun sebaliknya dipol sesaat atau dipol terimbas yang bermuatan negatif (ujung negatif) lebih dekat ke arah kation.
Walaupun demikian gaya yang terjadi antar molekul nonpolar dengan suatu sangat lemah. Hal inilah yang menyebabkan molekul polar cenderung melarutkan zat-zat yang bersifat ion, karena gaya molekul polar dengan ion lebih kuat dibanding molekul nonpolar. Sedangkan molekul nonpolar cenderung melarutkan molekul atau zat yang bersifat nonpolar.
Pengaruh Gaya Antarmolekul terhadap Sifat Fisis dan kimia zat
Gaya yang terjadi antarmolekul terutama gaya tarik apat mempengaruhi sifat dan kimia zat. Sifat fisika zat yang dipengaruhi gaya antarmolekul antara lain, titik didih, titik lebur, kalor penguapan viskositas. Sedangkan sifat kimia yang dipengaruhi oleh gaya antarmolekul terutama adalah sifat asam basa zat.
Titik didih, titik lebur, kalor penguapan makin besar atau makin tinggi bila gaya antarmolekul makin kuat, begitupun sebaliknya.
Viskositas atau kekentalan merupakan kemudahan suatu zat untuk mengalir. Semakin besar viskositas, maka zat tersebut semakin sukar mengalir, begitupun sebaliknya suatu zat akan semakin mudah mengalir bila viskositasnya kecil atau rendah. Contohnya air lebih mudah mengalir dibanding oli sehingga air memiliki viskositas yang lebih kecil atau lebih rendah dibanding oli.
Viskositas zat berkaitan dengan gaya antarmolekulnya. Bila gaya antarmolekul kuat zat memiliki viskositas tinggi begitupun sebaliknya. Oleh sebab itu, viskositas dipengaruhi oleh suhu, suhu makin tinggi viskositas zat akan menurun sehingga lebih mudah mengalir.
FILE ARTIKEL INI SILAKAN UNDUH DI SINI….!!!!!!
BEBERAPA ARTIKEL YANG DISARANKAN :
-
Kaidah Oktet dan Duplet
-
Penggolongan senyawa ionik
-
Kestabilan senyawa ionik apakah karena terpenuhinya aturan oktet?
-
Ikatan Kovalen
-
Struktur kristal beberapa senyawa ionik